삼플루오르화 붕소
"오늘의AI위키"의 AI를 통해 더욱 풍부하고 폭넓은 지식 경험을 누리세요.
1. 개요
삼플루오르화 붕소(BF3)는 평면 삼각 분자 구조를 가지는 무색 기체로, 루이스 산으로 작용하여 다양한 유기 반응의 촉매 및 반도체 공정의 도펀트로 사용된다. 붕소 산화물과 플루오르화 수소의 반응으로 제조되며, 1808년 조제프 루이 게이뤼삭과 루이 자크 테나르에 의해 처음 발견되었다. BF3는 전자쌍 받개로 작용하여 루이스 염기와 반응하여 부가물을 형성하며, 특히 유기 합성에서 불포화 화합물의 중합 개시, 이성화, 알킬화, 에스테르화, 축합 반응 등의 촉매로 활용된다. 또한, 이온 주입 공정 및 에피택셜 실리콘의 p형 반도체 도펀트로 사용되며, 중성자 검출기, 훈증제, 마그네슘 땜납 플럭스 등 다양한 용도로 활용된다.
더 읽어볼만한 페이지
- 산 촉매 - 인산
인산은 화학식 H₃PO₄를 가지며, 인광석을 이용한 습식 또는 건식 공정으로 생산되어 비료, 식품 첨가물, 세제, 의약품, 금속 처리 등 다양한 산업 분야에 사용되는 인 화합물이다. - 산 촉매 - 고체산
고체산은 알루미노규산염, 제올라이트, 유기산 등을 포함하는 고체 상태의 산으로, 산업 화학 공정 촉매 및 연료 전지 전해질로 사용되며 액체산이나 기체산에 비해 안정성과 재사용성이 높다는 장점을 가진다. - 붕소 화합물 - 질화 붕소
질화 붕소는 붕소와 질소의 화합물로, 다양한 결정 구조를 가지며, 높은 열적, 화학적 안정성과 우수한 윤활성을 바탕으로 절삭 공구, 연마재 등 다양한 분야에 응용된다. - 붕소 화합물 - 붕산
붕산은 붕소의 산화물로, 살충제, 난연제, 의약품 등 다양한 용도로 사용되며, 붕사에 무기산을 작용시켜 얻을 수 있고, 가열 시 산화 붕소로 분해되며, 루이스 산으로 작용하고, 과다 섭취 시 독성을 나타낼 수 있다. - 플루오린화물 - 헥사플루오로인산
- 플루오린화물 - 아불화 은
아불화 은은 아이오딘화 카드뮴과 결정 구조는 같지만 이온 위치가 반대이며, 은 원자 간 최단 거리는 299.6 pm이다.
2. 구조와 결합
삼플루오르화 붕소(BF3) 분자는 평면 삼각 분자 구조를 가진다. VSEPR 이론에 의해 예측되는 D3h 점군 대칭성을 가지며, 높은 대칭성으로 인해 쌍극자 모멘트는 0이다. 이 분자는 탄산염 음이온(CO32-)과 등전자체이다.[7] 붕소 원자는 sp2 혼성 오비탈을 형성한다.
붕소 삼할로겐화물(BX3)에서 B-X 결합 길이는 (1.30 Å)는 단일 결합에서 예상되는 것보다 짧다.[7] 이는 붕소와 플루오린 원자 사이에 부분적인 π 결합이 형성되기 때문이다. 붕소의 빈 2p 오비탈과 플루오린의 2p 오비탈이 겹쳐 π 결합을 형성한다.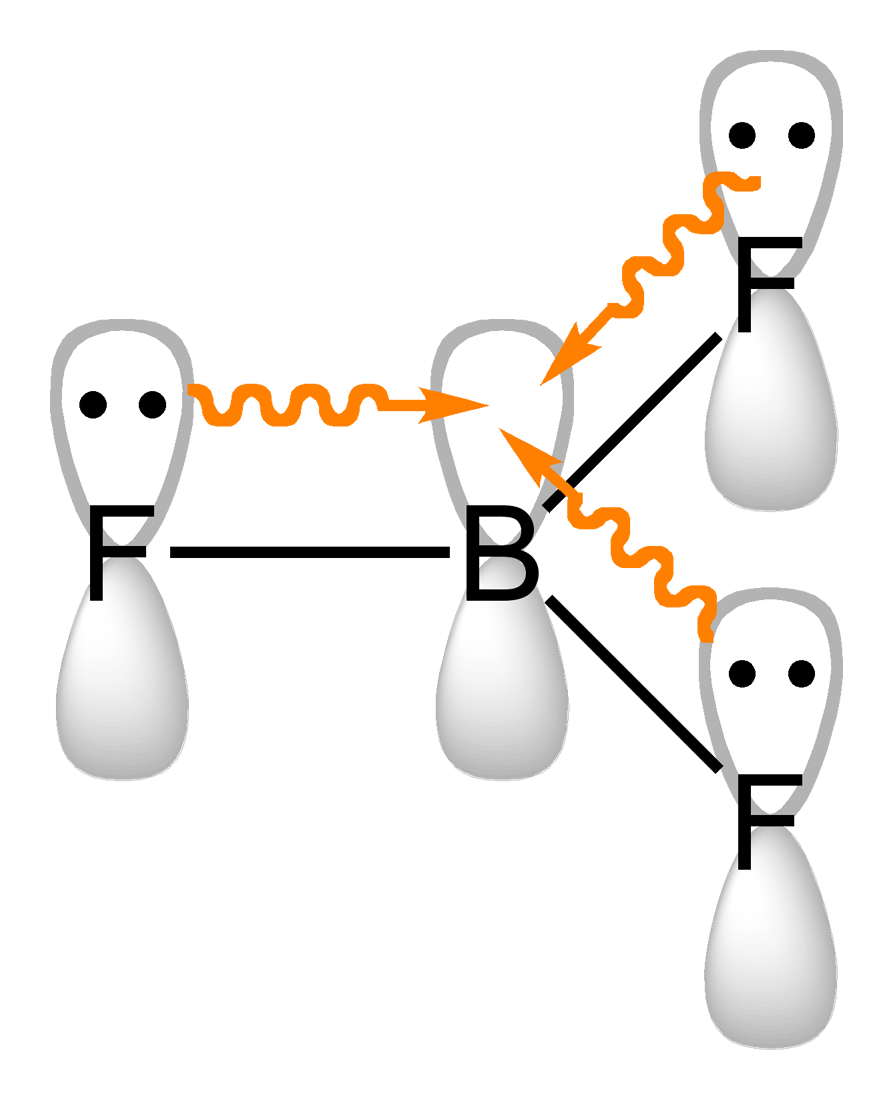
삼플루오르화 붕소의 공유 결합은 강하게 분극되어 있지만, 분자 자체는 비극성이다.
2. 1. 루이스 산성도
삼플루오르화 붕소(BF3)는 루이스 산으로, 전자쌍 받개로 작용하여 루이스 염기와 반응한다. 다른 붕소 삼할로겐화물(BCl3, BBr3, BI3)과 비교했을 때, BF3의 루이스 산성도는 가장 약하다.[17] 이는 B-F 결합의 강한 파이 결합으로 인해 붕소의 전자 부족 현상이 부분적으로 해소되기 때문이다.[1] F 원자가 더 큰 Cl 및 Br 원자에 비해 작다는 점을 고려하면, 붕소와 할로겐 사이의 결합 길이는 불소에서 요오드로 갈수록 증가하므로 궤도 함수의 공간적 중첩이 더 어려워진다.[1] F의 p''z''에 있는 비공유 전자쌍은 쉽게 기증되고 붕소의 빈 pz 궤도 함수와 중첩된다. 결과적으로 F의 파이 기증은 Cl 또는 Br보다 크다.[1]BF3는 루이스 염기와의 반응에서 부가물(adduct)을 형성하며, 대표적인 예로 플루오르화 세슘(CsF)과 반응하여 테트라플루오로붕산 세슘(CsBF4)을 생성한다.[15]
:
3. 합성 및 취급
삼플루오르화 붕소(BF3)는 붕소 산화물(B2O3)과 플루오르화 수소(HF)의 반응으로 제조된다.
::
일반적으로 플루오르화 수소는 황산과 형석(CaF2)으로부터 ''in situ'' 방식으로 만들어진다.[9] 매년 약 2300~4500톤의 삼플루오르화 붕소가 생산된다.[10]
실험실에서는 삼플루오르화 붕소 에테르 착물(BF3·OEt2)을 이용하여 삼플루오르화 붕소를 현장에서 생성한다. 이 착물은 액체 상태로 판매되어 취급이 용이하다.
용매가 없는 삼플루오르화 붕소를 얻는 방법으로는 테트라플루오로붕산 디아조늄 염의 열분해가 있다.[11]
::
테트라플루오르붕산 나트륨, 삼산화 붕소, 황산을 반응시켜 삼플루오르화 붕소를 생성할 수도 있다.[12]
::
3. 1. 성질 및 보관
무수 삼플루오르화 붕소는 끓는점이 −100.3 °C이고 임계 온도가 −12.3 °C이므로, 해당 온도 범위에서만 냉장 액체로 보관할 수 있다. 보관 또는 운송 용기는 내부 압력을 견딜 수 있도록 설계해야 한다. 냉장 시스템 고장 시 압력이 49.85 bar의 임계 압력까지 상승할 수 있기 때문이다.[13]삼플루오르화 붕소는 부식성이 있다. 삼플루오르화 붕소를 취급하는 장비에 적합한 금속으로는 스테인리스강, 모넬, 하스텔로이 등이 있다. 수분이 존재하면 스테인리스강을 포함한 강철을 부식시킨다. 폴리아미드와 반응하며, 폴리테트라플루오로에틸렌(테플론), 폴리클로로트리플루오로에틸렌, 폴리비닐리덴 플루오라이드, 폴리프로필렌은 만족스러운 내성을 보인다. 장비에 사용되는 구리스는 탄화수소 기반의 구리스와 반응하므로 플루오로카본 기반이어야 한다.[14]
4. 반응
삼플루오르화 붕소는 다른 붕소 삼할로겐화물(BCl3, BBr3)과 할로겐 교환 반응을 일으킨다.[15]
:
이러한 교환 반응이 쉽게 일어나기 때문에 혼합 할로겐화물은 순수한 형태로 얻을 수 없다.
삼플루오르화 붕소는 플루오르화물 및 에테르와 같은 루이스 염기와 부착물을 형성하는 다양한 루이스 산이다.[15]
:
:
테트라플루오로붕산염 염은 일반적으로 비배위 음이온으로 사용된다.
다이에틸 에테르와의 부착물인 삼플루오르화 붕소 다이에틸 에테르 착물(BF3·O(CH2CH3)2)은 편리하게 취급할 수 있는 액체이며, 실험실에서 BF3의 공급원으로 널리 사용된다.[15] 다이메틸 설파이드와의 부착물(BF3·S(CH3)2) 또한 순수한 액체로 취급할 수 있다.[16]
삼플루오르화 붕소는 물과 반응하여 붕산과 플루오로붕산을 생성한다. 반응은 아쿠오 부가물(H2O·BF3)의 형성으로 시작되며, 이후 HF를 잃으면서 플루오로붕산이 생성된다.[21]
:
더 무거운 삼할로겐화물은 사면체 이온 [BCl4]- 및 [BBr4]-의 낮은 안정성 때문에 위와 유사한 반응을 보이지 않는다. 플루오로붕산의 높은 산성도 때문에 플루오로붕산염 이온은 고체로 분리하기 어려운 다이아조늄 이온과 같이 특히 친전자성 양이온을 분리하는 데 사용될 수 있다.
삼플루오르화 붕소는 암모니아나 다이에틸 에테르 등의 루이스 염기와 복합체를 형성하기 쉽다. 특히 다이에틸 에테르와는 증류가 가능할 정도로 안정적인 착체를 만들며, 이 형태로 시판되기도 한다. 루이스 산 촉매로 유기 합성 분야에서 널리 사용된다.
5. 이용
삼플루오르화 붕소는 이온 주입 및 에피택셜 성장된 실리콘의 P형 반도체 도펀트로 사용되며, 고감도 중성자 검출기로도 사용된다.[12]
5. 1. 유기 화학
삼플루오르화 붕소는 주로 유기 합성에서 시약으로 사용되며, 일반적으로 루이스 산으로 사용된다.[10][22]- 불포화 화합물의 중합 반응 개시제로, 폴리에테르 등이 그 예이다.
- 이성질화, 아실화,[23] 알킬화, 에스터화, 탈수 반응,[24] 축합 반응, 무카이야마 알돌 반응 등 여러 반응의 촉매로 사용된다.[25]
5. 2. 반도체 산업
삼플루오르화 붕소는 이온 주입 공정에서 도펀트로 사용된다.[1] 또한 에피택셜 성장된 실리콘의 p형 반도체 도펀트로도 사용된다.[1]5. 3. 기타 용도
이온 주입 및 에피택셜하게 성장된 실리콘의 p형 반도체 도펀트로 사용된다.[12] 전리함과 지구 대기의 방사선 수준을 모니터링하는 장치에서 민감한 중성자 검출 및 고감도 중성자 검출기로 사용된다. 훈증 및 마그네슘 땜납의 플럭스로도 사용된다.[12] 다이보레인 제조, 불포화 결합을 가진 화합물의 중합 개시제, 그리고 이성화, 알킬화, 에스테르화, 축합 반응 등의 촉매로 사용된다.6. 발견
조제프 루이 게이뤼삭과 루이 자크 테나르는 1808년 플루오르화 칼슘과 유리화된 붕산을 결합하여 삼플루오르화 붕소를 발견했다. 이들은 불산(플루오르산)을 분리하려 했으나, 생성된 증기가 유리를 부식시키지 않아 "플루오붕산 가스"라고 명명했다.[26][27]
참조
[1]
서적
Prudent Practices in the Laboratory
http://www.nap.edu/o[...]
1995-08-16
[2]
간행물
CLP Regulation
[3]
간행물
[4]
간행물
[5]
간행물
Boron trifluoride
[6]
웹사이트
New Environment Inc. - NFPA Chemicals
http://www.newenv.co[...]
New Environment Inc
2018-05-07
[7]
서적
Chemistry of the Elements
Butterworth-Heinemann
[8]
논문
Covalent and Ionic Molecules: Why Are BeF2 and AlF3 High Melting Point Solids whereas BF3 and SiF4 Are Gases?
[9]
서적
Inorganic Chemistry
Academic Press
[10]
간행물
Boron Compounds
[11]
간행물
Fluorobenzene
[12]
서적
Handbook of Preparative Inorganic Chemistry
https://books.google[...]
Academic Press
1963
[13]
서적
Chemical Properties Handbook
McGraw-Hill
[14]
백과사전
Boron trifluoride
http://encyclopedia.[...]
Air Liquide
2016-12-15
[15]
서적
Encyclopedia of Reagents for Organic Synthesis
[16]
서적
Encyclopedia of Reagents for Organic Synthesis
[17]
간행물
Cotton&Wilkinson6th
[18]
논문
Group V Chalcogenide Complexes of Boron Trihalides
[19]
논문
A Computational Analysis of the Bonding in Boron Trifluoride and Boron Trichloride and their Complexes with Ammonia
[20]
문서
Here on Wikipedia an easy to understand table is found, which shows drawings of the several higher p orbitals.
[21]
논문
Equilibria in the System Boron Trifluoride–Water at 25°
[22]
논문
[23]
논문
Boron Trifluoride in the Synthesis of Plant Phenolics: Synthesis of Phenolic Ketones and Phenyl Stryl Ketones
http://www.tennacado[...]
1991
[24]
논문
Organic Reactions with Boron Fluoride. IX. The Alkylation of Phenol with Alcohols
1935
[25]
웹사이트
Boron Trifluoride (BF3) Applications
http://www51.honeywe[...]
Honeywell
[26]
논문
Sur l'acide fluorique
[27]
논문
Des propriétés de l'acide fluorique et sur-tout de son action sur le métal de la potasse
https://books.google[...]
[28]
문서
Index no. 005-001-00-X of Annex VI, Part 3, to Regulation (EC) No 1272/2008 of the European Parliament and of the Council of 16 December 2008 on classification, labelling and packaging of substances and mixtures, amending and repealing Directives 67/548/EEC and 1999/45/EC, and amending Regulation (EC) No 1907/2006. OJEU L353, 31.12.2008, pp 1–1355 at p 341.
http://eur-lex.europ[...]
[29]
문서
"Boron trifluoride"
http://www.cdc.gov/n[...]
[30]
문서
毒物及び劇物指定令 昭和四十年一月四日 政令第二号 第一条 六の十一
http://wwwhourei.mhl[...]
[31]
웹사이트
Air Liquide Gas Encyclopaedia
http://encyclopedia.[...]
[32]
서적
Prudent Practices in the Laboratory
http://www.nap.edu/o[...]
2018-05-07
[33]
간행물
CLP Regulation
[34]
간행물
[35]
간행물
[36]
IDLH
Boron trifluoride
[37]
웹인용
New Environment Inc. - NFPA Chemicals
http://www.newenv.co[...]
2018-05-07
본 사이트는 AI가 위키백과와 뉴스 기사,정부 간행물,학술 논문등을 바탕으로 정보를 가공하여 제공하는 백과사전형 서비스입니다.
모든 문서는 AI에 의해 자동 생성되며, CC BY-SA 4.0 라이선스에 따라 이용할 수 있습니다.
하지만, 위키백과나 뉴스 기사 자체에 오류, 부정확한 정보, 또는 가짜 뉴스가 포함될 수 있으며, AI는 이러한 내용을 완벽하게 걸러내지 못할 수 있습니다.
따라서 제공되는 정보에 일부 오류나 편향이 있을 수 있으므로, 중요한 정보는 반드시 다른 출처를 통해 교차 검증하시기 바랍니다.
문의하기 : help@durumis.com

